
近日,上海交通大学医学院公共卫生学院和单细胞组学与疾病研究中心王慧教授员团队和复旦大学中山医院刘厚宝教授团队在国际知名医学期刊《Clinicaland Translational Medicine》(IF=11.492)在线发表了题为“Diversity and intratumoral heterogeneity in human gallbladder cancerprogression revealed by single-cell RNA sequencing” 的论文。该研究利用BD Rhapsody™ 平台的单细胞测序技术全面解析了胆囊癌图谱,分别从癌细胞异质性、肿瘤微环境细胞浸润、活性以及相互作用等多个方面全面表征了胆囊癌组织的疾病特征,为胆囊癌中免疫微环境功能解析及其新治疗方案的研究提供了新的视角。

课题研究背景
胆囊癌是一种起病隐匿,恶性程度高、侵袭性强的恶性肿瘤,发病率低但死亡率高,5年生存率不到5%。尽管化疗、靶向治疗和免疫疗法为患者提供了治疗选择,但仅有少数患者反应良好。前期基于二代测序、微阵列等研究手段确定了可能导致肿瘤发生和进展的热点突变或异常表达的基因,然而这些因素只占了一小部分,对于临床靶向治疗的支持有限。本研究首次利用单细胞测序技术对原发性、淋巴结转移性肿瘤组织以及邻近正常胆管组织的肿瘤微环境进行全面解析,通过深入了解胆囊癌组织的肿瘤异质性,确定细胞特征,提高对胆囊癌发生和进展过程的理解,进一步为胆囊癌提供新的治疗策略。
研究整体思路
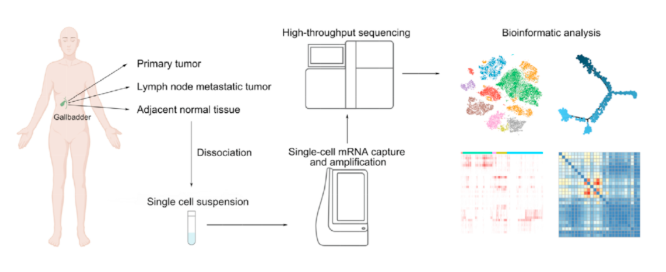
实验设计亮点
疾病分型全面
该研究的患者囊括了胆囊癌常见、罕见的3种亚型,总体5名患者,包含3位胆囊腺癌患者、1位胆囊腺鳞状细胞癌(ADC)患者,1位胆囊神经内分泌肿瘤(NET)患者。
组织类型丰富
每位患者取不同的组织,总体包括原发性胆囊癌组织,淋巴结转移瘤组织,以及邻近的正常组织。
样本多标检测
每位患者取的多种组织,通过BD平台多样本标记的方法,每个样本标记特有的Tag标签混合在一起进行上机捕获,有效的降低了批次效应。
生信分析结论
肿瘤起源
胆囊内分泌肿瘤起源与胆囊癌腺癌和鳞癌显著不同,其肿瘤微环境中很少存在淋巴细胞和髓系细胞浸润,而是以基质细胞为主。
免疫微环境
以耗竭型的T细胞(TIGIT+,GTLA4+)和APOE+巨噬细胞为特征的免疫抑制微环境,可能是机体对免疫耐受的主要原因。
细胞通讯网络
原发性胆囊癌细胞、内皮细胞和巨噬细胞之间存在显著的的配体-受体介导的相互作用关系。
主要结果展示
胆囊癌上皮肿瘤细胞和神经内分泌肿瘤细胞的异质性
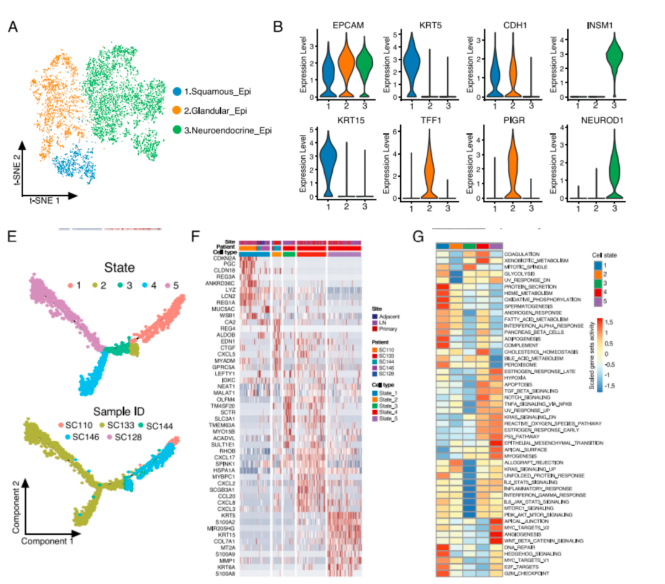
利用BD Rhapsody™单细胞全转录测序技术共捕获了24887个细胞及所有的转录本,包括原发肿瘤组织(9040个细胞),淋巴结转移瘤组织(8917个细胞),邻近正常组织(6930个细胞)。通过TSNE分析和特征性Marker gene的表达鉴定出10种细胞类型。从比例来看,CDH1/EPCAM+上皮细胞在腺癌和鳞状细胞癌组织中富集,而在NET组织中较少,NET更多富集的是EPCAM+/INSM1神经内分泌细胞。从功能上看,整合EPCAM+上皮细胞和NET细胞单独进行分析,通过不同的Marker gene鉴定了3个细胞簇,把其中鉴定的CDH1+的上皮细胞再分成几个亚簇,分别是KRT5、KRT15、KRT6A 和 KRT17角蛋白高表达的鳞状细胞,分泌蛋白和细胞因子TFF1,LCN2高表达的腺上皮细胞。通过GSEA富集分析进一步揭示了不同细胞类型的异质性,NET细胞在增值、DNA合成、嘌呤生物合成功能中显著富集,腺细胞表现出更强的胆酸代谢、胆固醇代谢、蛋白质分泌活性,而鳞状细胞在这方面表现相对减弱。这些差异解释了不同类型的肿瘤和微环境的异质性。

胆囊癌肿瘤细胞具有高度异质性,腺癌具有向鳞癌分化的潜能
对腺癌和腺鳞癌患者的上皮细胞进行拟时序分析,可分为5个不同的时段,从样本的角度看,大多数的上皮细胞都是来源于腺鳞癌的患者,对腺鳞癌患者的不同种类的肿瘤细胞进行分析,可看出腺上皮细胞处于早期阶段,腺鳞状上皮肿瘤细胞处于晚期阶段,如果对于每个亚群的特征性marker gene进行GSEA富集,基因所在的生物过程展示了鳞癌肿瘤中腺癌具有向鳞癌转化的趋势,生物学过程表现为表皮发育、角质化活动的增加。
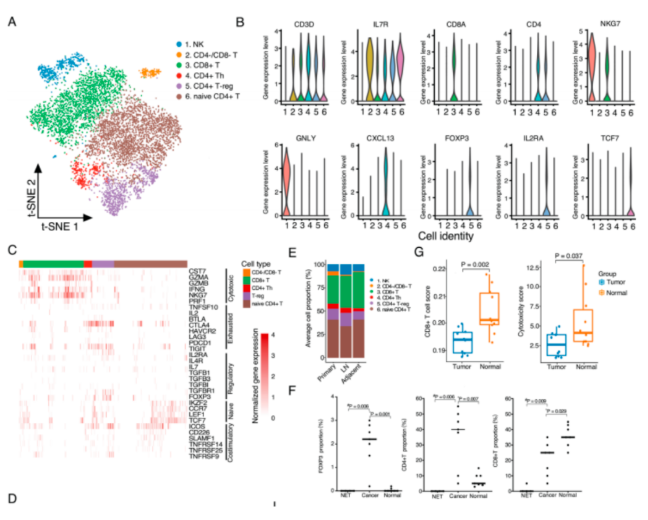
肿瘤组织出现免疫抑制微环境
通过对T/NK细胞亚群中肿瘤和正常组织的对比,发现原发性、淋巴结转移的组织中CD4+Th和CD4+T-reg细胞的比例增加,而浸润的CD8+T细胞水平较低,免疫组化进一步证实了该结果。公共数据集(GSE139682)中10对胆囊癌和正常组织的免疫浸润分析也表明CD8+ Tcell免疫浸润和细胞毒性的评分较低,与本研究结果一致。
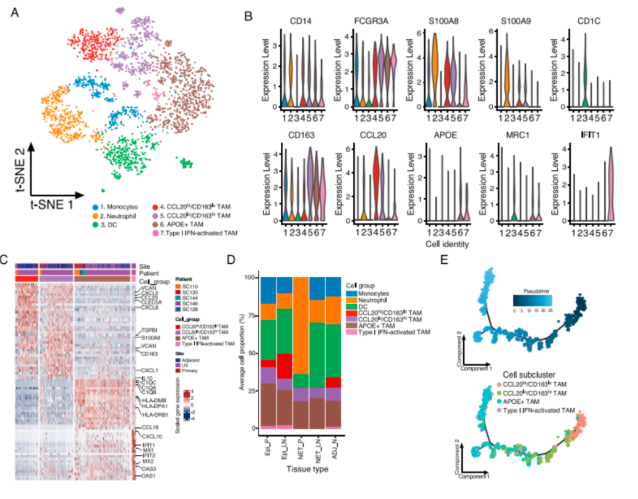
原发性胆囊肿瘤组织中巨噬细胞的轨迹发生转变
髓样细胞在抗原呈递和炎症作用中起到关键性的作用,其中最为丰富的巨噬细胞可以被分为4个亚群,为了描绘巨噬细胞的转变,采用无监督的轨迹分析,发现CCL20hi/CD163lo、CCL20lo/CD163hi、T1-IFN亚型的巨噬细胞持续性的向APOE+ 巨噬细胞发生转变,GO富集分析也发现了IFN-γ通路的响应,淋巴细胞活化的正调节和淋巴细胞分化的增加,与此同时,白细胞的趋化性、IL-6产生等在减少。
基质细胞和内皮细胞的重塑与胆囊癌组织中的血管生成相关
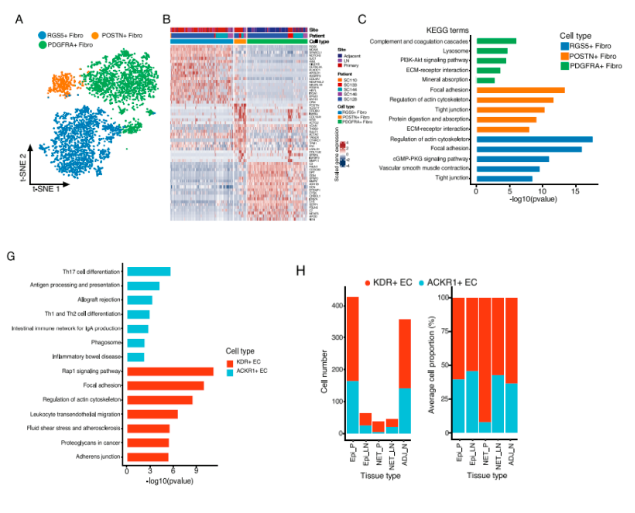
在scRNA-seq聚类出的10个细胞类型中,把成纤维细胞单独拿出可以细分为3类亚群,在原发/淋巴结转移的胆囊癌组织中,PDGFRA+成纤维细胞显着减少,PSOTN+和 RGS5+成纤维细胞显著增加,这一结果与正常组织的情况正好相反。而以细胞外基质基因高表达为特征的PSOTN+成纤维细胞的显著增加,通过KEGG分析,表明与高蛋白质的消化和吸收相关。内皮细胞确定了2个细胞亚群,KDR+ (VEGFR-2)和 ACKR1+ 内皮细胞,KDR+(VEGFR-2)和Flt-1(VEGFR-1)作为血管生成因子 VEGFA 和 VEGFB 的受体都在KDR+内皮细胞中高表达,ACKR1+作为非典型的趋化因子的受体,可以活化趋化因子从而促使骨髓细胞和白细胞在肿瘤组织中富集,该亚型的内皮细胞在肿瘤组织中有所增加。综上表明,基质细胞和内皮重塑可能会增强肿瘤组织中的血管生成。
原发性胆囊癌细胞间配体-受体相互作用
使用CellPhoneDB 算法构建细胞网络,与腺癌相比,鳞状细胞癌中通过MIF/TNFRSF10D, EGFR/GRN, EGFR/HBEGF和 EPHB2/EFNB2下显示出内皮细胞内有更强的通讯,值得注意的是,ACKR+内皮细胞和抗炎巨噬细胞在原发性和淋巴结转移的组织中相互作用明显增强,提示着这样的互作可能会有助于巨噬细胞的募集与状态转变。

科学发现小结
该研究详细阐述了原发性胆囊癌、腺鳞癌和胆囊神经内分泌肿瘤(NET)的细胞图谱以及它们的差异,腺癌细胞失去了呈递抗原的 MHC II 分子,可以转分化为鳞状肿瘤细胞,原发性胆囊癌中的免疫抑制性 TME 由浸润的 CD4+T-reg、CXCL13+Th 细胞、CCL201o/cD163hi 和 APOE+巨噬细胞组成,然而,他们却是 NET 的免疫沙漠表型。重塑GC组织中的基质和内皮细胞促进血管生成和淋巴管生成以维持GC的生长和转移。以上工作解决了胆囊癌组织的单细胞转录组学分析,提示靶向肿瘤免疫微环境和血管发生可能是胆囊癌上皮细胞癌的有效治疗手段,并从细胞和分子角度都提供了新的潜在靶点。
参考文献
Chen P , Wang Y , Li J , et al. Diversity and intratumoral heterogeneity in human gallbladder cancer progression revealed by singleヽell RNA sequencing[J]. Clinical and Translational Medicine, 2021, 11(6).
DOI:10.1002/ctm2.462


