英文题目:Osteoclast-derived apoptotic bodies show extended biological effects of parental cell in promoting bone defect healing
中文题目:破骨细胞来源的凋亡小体在促进骨缺损愈合中的作用
期刊:Theranostics
IF:8.063
合作单位:第三军医大学西南医院
本研究RNAseq部分由中科普瑞协助完成
研究意义
凋亡小体(ABs)是包裹死细胞残余成分的一种细胞外囊泡(Extracellular vesicles, EVs),因其在细胞间通讯中的潜在作用而受到越来越多的关注。在骨转换,骨吸收阶段结束时,大部分破骨细胞发生凋亡,产生大量的ABs,但破骨细胞来源的ABs在骨重塑中的作用尚不清楚。
研究方法
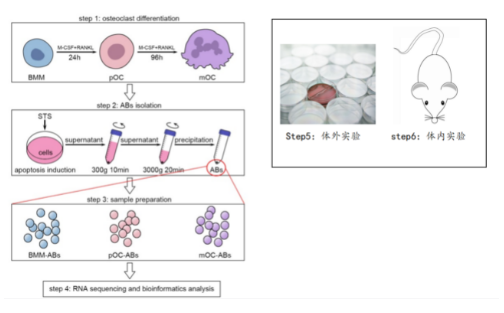
本研究通过Staurosporine诱导细胞凋亡,差异离心法分离ABs, 接着利用Western blotting、流式细胞术、透射电镜(透射电镜)鉴定ABs, 全转录组测序检测破骨细胞来源的ABs不同阶段的转录组水平变化。采用VENN分析和基因集富集分析(gene set enrichment analysis, GSEA)比较ABs与亲代细胞表达谱的相似性。体外通过血管形成实验和碱性磷酸酶染色观察ABs对血管生成和成骨的影响。体内实验利用颅骨缺损小鼠模型来评估ABs修饰的脱钙骨基质(DBM)支架对血管生成和成骨的影响。
研究结论
通过测序结果绘制了破骨细胞来源的ABs在不同分化阶段的RNA表达图谱,通过与亲代破骨细胞RNA表达谱的比较,发现ABs的转录组与相应亲代细胞有很高的相似性。体外和体内的功能研究表明,与亲本细胞相似,pOC-ABs增强了内皮祖细胞的增殖和分化,而mOC-ABs促进了成骨分化。ABs的遗传生物学效应是由几个关键lncRNA介导的,对这些lncRNA的干扰可消除了AB的功能。
研究主要结果
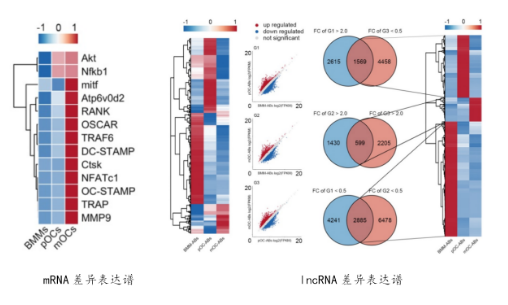
— 表达谱数据分析
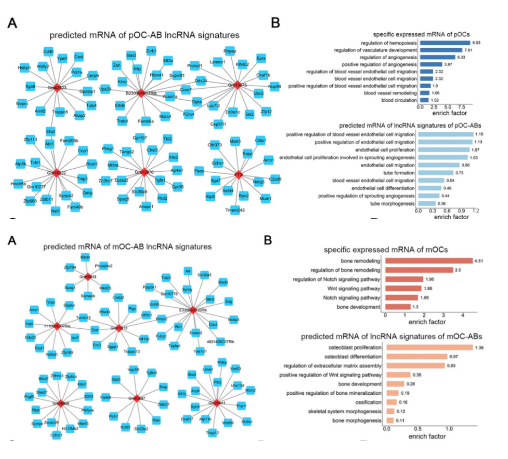
按亲本细胞分化阶段建立3个比较组,分别为: pOC-ABs vs BMM-ABs (G1)、mOC-ABs vs BMM-ABs (G2)、mOC-ABs vs pOC-ABs (G3)。RNA测序分析BMM、pOC和mOC的差异基因表达谱,差异lncRNA表达谱。因为ABs中的mRNA很少被翻译,ABs中的mRNA更多的反映的是亲本细胞的基因表达模式,并不是它们自身的功能;而LncRNA通过囊泡转运发挥着重要的调控作用,为了了解破骨细胞衍生的ABs的生物学功能,本次研究将重点放在lncRNA上。
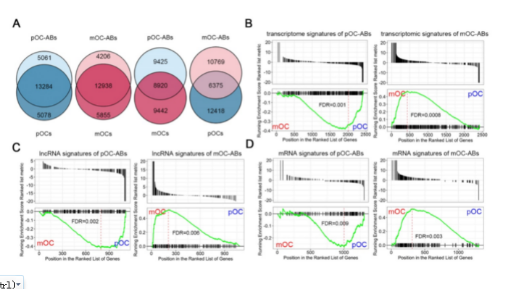
— 破骨细胞来源的ABs和相应亲本细胞的转录相似性
对破骨细胞来源ABs与相应亲本细胞(pOC和mOC)之间所有RNA的数据进行了VENN分析。结果显示,ABs与其亲代细胞的重叠RNA部分约为75%。GSEA分析发现,pOC-AB转录组特征与pOC表型相似,而mOC-AB更倾向于表现为mOC表型。利用GSEA,进一步鉴定了ABs的lncRNA/mRNA表达也与亲本细胞高度相似。
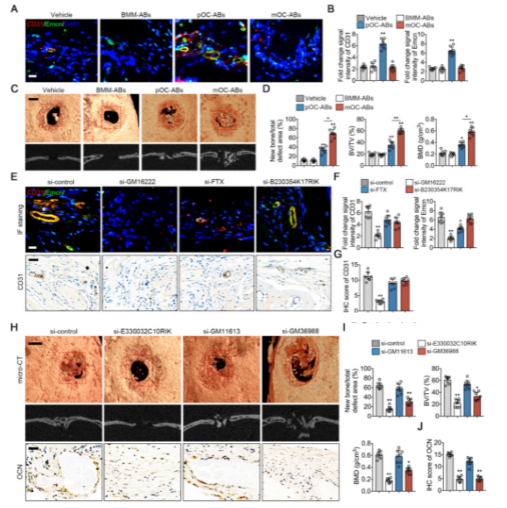
— ABs与亲代破骨细胞的功能相似性由关键lncRNA介导的
对lncRNA的靶基因进行预测及功能分析,发现pOC-ABs可能与亲代细胞具有类似的促血管生成作用,mOC-Abs与成骨功能相关。定量验证得到3个lncRNA,通过体外敲降实验验证相关功能。功能实验证明了几个关键的lncRNA决定了ABs在血管生成和成骨中的生物学作用,其缺失会导致相应功能的减弱或丧失。
— 体内实验证明,pOC-ABs可诱导血管生成,mOC-ABs可促进成骨
通过颅骨缺损小鼠进行体内实验,验证pOC-ABs的促血管生成能力和mOC-ABs的成骨潜能,结果与体外实验一致。